‹@ٹBگفŒvژز‚ة•K—v‚ب”M—حٹw‚ج’mژ¯‚ئŒvژZ”\—ح‚ًگg‚ة‚آ‚¯‚ç‚ê‚éپIƒGƒ“ƒ^ƒ‹ƒsپAƒGƒ“ƒgƒچƒsپAƒGƒNƒZƒ‹ƒM‚ئ‚¢‚ء‚½ڈd—v‚بٹT”O‚ًگ[‚—‰ً‚µپA‹ï‘ج“I‚بƒTƒCƒNƒ‹‚ئ‹¤‚ةگفŒv‚ة‰—p‚·‚é—ح‚ً—{‚¦‚éپB
”M—حٹw‘و“ٌ–@‘¥
’†‰›‚ةژdگط”آ‚ج‚ ‚éگ…‘…‚جچ¶‰E‚ة پu20پژ‚جگ…پv ‚ئ پu90پژ‚ج‚¨“’پv ‚ھ“ü‚ء‚ؤ‚¢‚ـ‚·پB
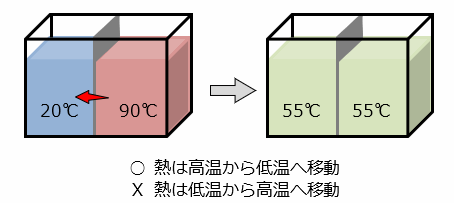
ژdگط”آ‚ً“`‚ء‚ؤ”M‚حˆع“®‚µ‚ـ‚·‚ھپAپu20پژ‚جگ…پv ‚©‚ç پu90پژ‚ج‚¨“’پv ‚ج•û‚ض”M‚حˆع“®‚µ‚ـ‚¹‚ٌپB•K‚¸”M‚حچ‚‚¢‰·“xپi90پژپj‚©‚ç’ل‚¢‰·“xپi20پژپj‚ضˆع“®‚µ‚ـ‚·پB
‚±‚ج‚و‚¤‚ة‹t‚ة‚ب‚ç‚ب‚¢پu•s‰آ‹t“I‚بŒ»ڈغپv‚ج‚±‚ئ‚ًپ@پu”M—حٹw‘و“ٌ–@‘¥پvپ@‚ئ‚¢‚¢‚ـ‚·پD

پ@”M‚ح”M‚¢‚à‚ج‚©‚ç—₽‚¢‚à‚ج‚ضˆع“®‚·‚é‚ھپA‚»‚ج‹t‚حگ¬—§‚µ‚ب‚¢پB
”M—حٹw‘و“ٌ–@‘¥‚حپAژں‚ج3‚آ‚جŒ´—‚â–@‘¥‚إگà–¾‚³‚ê‚ـ‚·پB
‚PپDƒGƒ“ƒgƒچƒsپ[‘‘ه‚ج–@‘¥
‚QپDƒNƒ‰ƒEƒWƒEƒX‚جŒ´—
‚RپDƒgƒ€ƒ\ƒ“‚جŒ´—
‚PپDƒGƒ“ƒgƒچƒsپ[‘‘ه‚ج–@‘¥
ƒGƒ“ƒgƒچƒsپ[‚ئ‚حپAپu•ھژq‚ج—گژG‚³پv ‚ج‚±‚ئ‚إ‚·پB
—ل‚¦‚خپAگ…‚ج’†‚ةƒCƒ“ƒN‚ً‚P“Hگ‚‚炵‚ـ‚·پBƒCƒ“ƒN‚حگ‚‚炵‚½ˆت’u‚©‚çچL‚ھ‚è‚ـ‚·پB
‚µ‚©‚µپAچL‚ھ‚ء‚½ƒCƒ“ƒN‚ھˆê‰سڈٹ‚ةڈW‚ـ‚ء‚ؤ‚‚邱‚ئ‚ح‚ ‚è‚ـ‚¹‚ٌپB

ƒCƒ“ƒN‚ج•ھژq‚حپA—گژG‚ب•ûŒü‚ض‘‘ه‚µ‚ؤ‚¢‚«‚ـ‚·پB
‚±‚ê‚ًپuƒGƒ“ƒgƒچƒsپ[‚ھ‘‘ه‚·‚éپv‚ئ‚¢‚¢‚ـ‚·پB
‚QپDƒNƒ‰ƒEƒWƒEƒX‚جŒ´—
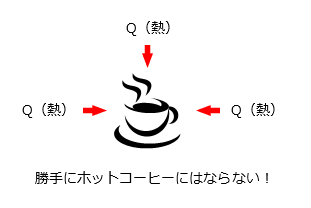
ƒNƒ‰ƒEƒWƒEƒX‚جŒ´—‚ئ‚حپAپuٹO•”‚©‚牽‚à•د‰»‚ً—^‚¦‚¸‚ة’ل‰·‚©‚çچ‚‰·‚ض”M‚ًˆع‚·‚±‚ئ‚ھ‚إ‚«‚ب‚¢پv‚ئ‚¢‚¤Œ´—‚إ‚·پB—ل‚¦‚خپA—â‚ك‚½ƒRپ[ƒqپ[‚ھپAٹO•”‚ج”M‚ً‹zژû‚µ‚ؤƒzƒbƒgƒRپ[ƒqپ[‚ة‚ح‚ب‚ç‚ب‚¢‚ئ‚¢‚¤‚±‚ئ‚إ‚·پB
‚RپDƒgƒ€ƒ\ƒ“‚جŒ´—پiƒPƒ‹ƒrƒ“‚ج–@‘¥پj
ƒgƒ€ƒ\ƒ“‚جŒ´—‚ئ‚حپAپuˆê‚آ‚ج”MŒ¹‚©‚ç”M‚ًژَ‚¯ژو‚èپC‚»‚ج‚·‚ׂؤ‚ًژdژ–‚ة•دٹ·‚·‚邱‚ئ‚ح•s‰آ”\‚إ‚ ‚éپv‚ئ‚¢‚¤Œ´—‚إ‚·پB
‚آ‚ـ‚èپAپu”M‚ج‘S‚ؤ‚ً‰^“®‚ئ‚µ‚ؤژو‚èڈo‚·‚±‚ئ‚ح‚إ‚«‚ب‚¢پv ‚ئ‚¢‚¤‚±‚ئ‚إ‚·پB—ل‚¦‚خپAژ©“®ژش‚جƒGƒ“ƒWƒ“‚إگà–¾‚µ‚ـ‚·‚ئپAƒGƒ“ƒWƒ“‚حƒKƒ\ƒٹƒ“‚ً”R‚₵‚½ پu”Mپv ‚©‚ç پuƒsƒXƒgƒ“‰^“®پv ‚ة•دٹ·‚µ‚ـ‚·‚ھپA‚P‚O‚Oپ“ƒsƒXƒgƒ“‰^“®‚ة•د‚¦‚邱‚ئ‚ح‚إ‚«‚ـ‚¹‚ٌپBˆê•”‚ھ•K‚¸ پu”r”Mپv ‚ئ‚µ‚ؤ”rڈo‚³‚ê‚ـ‚·پB
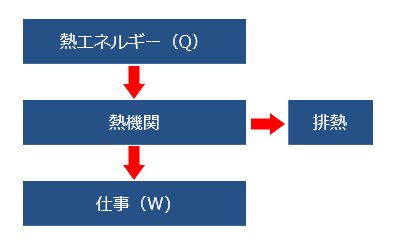
چ‚‰·‚ج”MƒGƒlƒ‹ƒMپ[‚©‚çژdژ–‚ًژو‚èڈo‚·‚ة‚حپA’ل‰·‚ج”MŒ¹‚ة”M‚ًژج‚ؤ‚ب‚¯‚ê‚خ‚ب‚è‚ـ‚¹‚ٌپBپu”M‚ً‘S‚ؤژdژ–‚ة•د‚¦‚é”M‹@ٹض‚ح‘¶چف‚µ‚ب‚¢پv ‚ئ‚¢‚¤‚ج‚ھ ƒgƒ€ƒ\ƒ“‚جŒ´— ‚إ‚·پB
ˆبڈم‚ج‚و‚¤‚ة”M—حٹw‘و“ٌ–@‘¥‚حپAژ„’B‚جگg‹ك‚إ‹N‚±‚錻ڈغ‚ئˆê’v‚µ‚ؤ‚¢‚ـ‚·پBپu‚ب‚؛پA‚»‚¤‚ب‚é‚ج‚©پHپv‚و‚èپAژ©‘R‚ة‹N‚±‚éŒoŒ±‘¥‚إ‚ ‚é‚ئ‘¨‚¦‚邱‚ئ‚ھ‘هگط‚إ‚·پB
“ئژ©ٹJ”‚³‚ꂽMONOڈm‚جپuƒXƒeƒbƒvژ®ٹwڈKƒvƒچƒOƒ‰ƒ€پvپƒ–@گlچج—pژہگرپF‚V‚O‚Oژذˆبڈمپ„
ƒJƒeƒSƒٹپ[ƒپƒjƒ…پ[
 ‹@ٹBگفŒv‚جٹî‘b‚ًٹw‚ش
‹@ٹBگفŒv‚جٹî‘b‚ًٹw‚ش
 ‚RDCA‚جٹî‘b‚ًٹw‚ش
‚RDCA‚جٹî‘b‚ًٹw‚ش
 چق—؟—حٹw‚جٹî‘b‚ًٹw‚ش
چق—؟—حٹw‚جٹî‘b‚ًٹw‚ش
 —¬‘ج—حٹw‚جٹî‘b‚ًٹw‚ش
—¬‘ج—حٹw‚جٹî‘b‚ًٹw‚ش
 ‹àŒ^‚جٹî‘b‚ًٹw‚ش
‹àŒ^‚جٹî‘b‚ًٹw‚ش
 ‹@ٹB‰ءچH‚جٹî‘b‚ًٹw‚ش
‹@ٹB‰ءچH‚جٹî‘b‚ًٹw‚ش
 ‹@ٹB—v‘f‚جٹî‘b‚ًٹw‚ش
‹@ٹB—v‘f‚جٹî‘b‚ًٹw‚ش
 ‚RDƒvƒٹƒ“ƒ^پ[‚جٹî‘b‚ًٹw‚ش
‚RDƒvƒٹƒ“ƒ^پ[‚جٹî‘b‚ًٹw‚ش
 ‹à‘®چق—؟‚جٹî‘b‚ًٹw‚ش
‹à‘®چق—؟‚جٹî‘b‚ًٹw‚ش
 گ»گ}‚جٹî‘b‚ًٹw‚ش
گ»گ}‚جٹî‘b‚ًٹw‚ش
 ‚RDCAD‚ج‰—p‚ًٹw‚ش
‚RDCAD‚ج‰—p‚ًٹw‚ش
 ”M—حٹw‚جٹî‘b‚ًٹw‚ش
”M—حٹw‚جٹî‘b‚ًٹw‚ش
 ‹@ٹB—حٹw‚جٹî‘b‚ًٹw‚ش
‹@ٹB—حٹw‚جٹî‘b‚ًٹw‚ش
 ‹àŒ^‚جژہ‘H‚ًٹw‚ش
‹àŒ^‚جژہ‘H‚ًٹw‚ش
 ‹àŒ^گ»چى‚T‚آ‚جƒ|ƒCƒ“ƒg
‹àŒ^گ»چى‚T‚آ‚جƒ|ƒCƒ“ƒg
 CAE‰ًگح‚جٹî‘b‚ًٹw‚ش
CAE‰ًگح‚جٹî‘b‚ًٹw‚ش
 ƒvƒ‰ƒXƒ`ƒbƒN‚جٹî‘b‚ًٹw‚ش
ƒvƒ‰ƒXƒ`ƒbƒN‚جٹî‘b‚ًٹw‚ش
 “d‹C‚جٹî‘b‚ًٹw‚ش
“d‹C‚جٹî‘b‚ًٹw‚ش
ƒXƒ|ƒ“ƒTپ[ƒh ƒٹƒ“ƒN